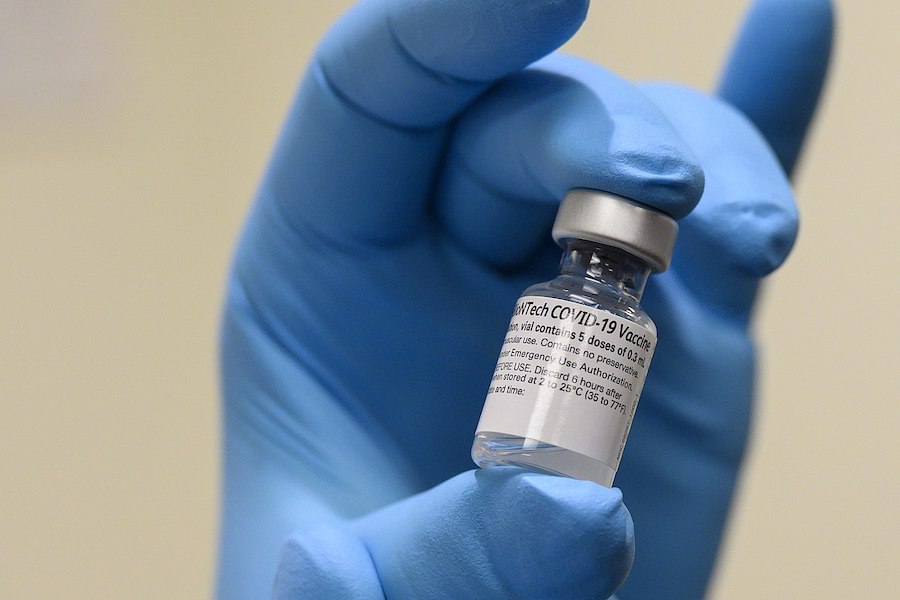
Le 23 août, Pfizer a annoncé sur son site Web que le vaccin Pfizer-BioNTech COMIRNATY avait reçu l’approbation complète de la Food and Drug Administration (FDA) aux Etats-Unis, pour les personnes âgées de 16 ans et plus. Même si la décision a été saluée par plusieurs médias, peu d’entre eux ont fourni une analyse critique des données ou ont abordé la question de savoir, en premier lieu, si l’approbation était justifiée.
Dans un article d’opinion paru récemment, la revue médicale The BMJ souligne les principales considérations qui auraient dû être prises en compte par la FDA avant l’octroi de l’autorisation.
Des données obsolètes
L’approbation complète de tout vaccin devrait toujours tenir compte des données les plus récentes disponibles afin de fournir au public les informations les plus précises et les plus sûres.
Le 28 juillet , sur le site medRxiv consacré à la recherche médicale, Pfizer et BioNTech ont publié les résultats actualisés sur l’innocuité et l’efficacité du vaccin suite à leur étude multinationale de phase 3 contrôlée par placebo et en aveugle sur la Covid-19. Cette étude impliquait 44 165 participants âgés de 16 ans et plus. L’efficacité du vaccin (VE) a été estimée à 91,3 % jusqu’à six mois.
Il est intéressant de noter que, quatre mois auparavant, ces entreprises avaient publié un communiqué de presse affichant une date limite identique pour les données, soit le 13 mars 2021. La principale conclusion de l’étude était la même, à savoir que l’efficacité du vaccin était de 91,3 % contre la Covid-19 symptomatique « jusqu’à six mois de suivi ».
Dans son communiqué de presse, Pfizer indique : « Pour l’approbation de la FDA, Pfizer et BioNTech ont soumis un ensemble complet de données comprenant des données de suivi à plus long terme de l’essai de phase 3, où l’efficacité élevée du vaccin et son profil de sécurité favorable ont été observés jusqu’à six mois après la deuxième dose. »
Toutefois, l’expression « données de suivi à plus long terme » est trompeuse, car ce sont les mêmes données de suivi à 6 mois qui ont été fournies à la FDA, et non des données de suivi à 10 mois.
Diminution de l’immunité
William Gruber, vice-président senior de Pfizer et l’un des auteurs de l’étude publiée par la société le 28 juillet dans medRxiv, a déclaré devant le comité consultatif de la FDA en décembre 2020 : « Nous allons examiner très attentivement la durabilité de la protection »
Une préoccupation majeure pour les vaccins est la diminution de leur efficacité au fil du temps, un phénomène bien connu de mutation rapide des virus respiratoires, comme le virus de la grippe. Une publication d’août 2018 dans la revue médicale Clinical Infectious Diseases a compilé les résultats de plusieurs études scientifiques, dont beaucoup ont montré une chute drastique de l’efficacité des vaccins antigrippaux à près de 20%, voire 0%, après 3 ou 4 mois post-vaccination.
Ainsi, les personnes qui se font vacciner tôt peuvent avoir une protection proche de zéro lorsque la saison de la grippe arrive des mois plus tard. De même, pour les vaccins Covid-19, la durée de la protection est une considération importante.
La FDA indique que l’efficacité d’un vaccin dans un essai d’efficacité contrôlé par placebo doit « être d’au moins 50 % ». Cependant, le ministère israélien de la santé a déclaré qu’au 5 juillet, l’efficacité du vaccin Pfizer-BioNTech « dans la prévention de l’infection et de la maladie symptomatique est tombée à 64% depuis le 6 juin ».
En outre, d’après une analyse effectuée entre le 20 juin et le 17 juillet en Israël, l’efficacité du vaccin avait chuté à seulement 39 % à la fin du mois de juillet, selon un rapport de CNBC. Compte tenu de la baisse de l’immunité, Israël a commencé à administrer une troisième injection aux adultes de plus de 40 ans. L’administration Biden, elle a prévu que « chaque adulte reçoive une injection de rappel huit mois après avoir reçu sa deuxième injection » à partir de la semaine du 20 septembre.
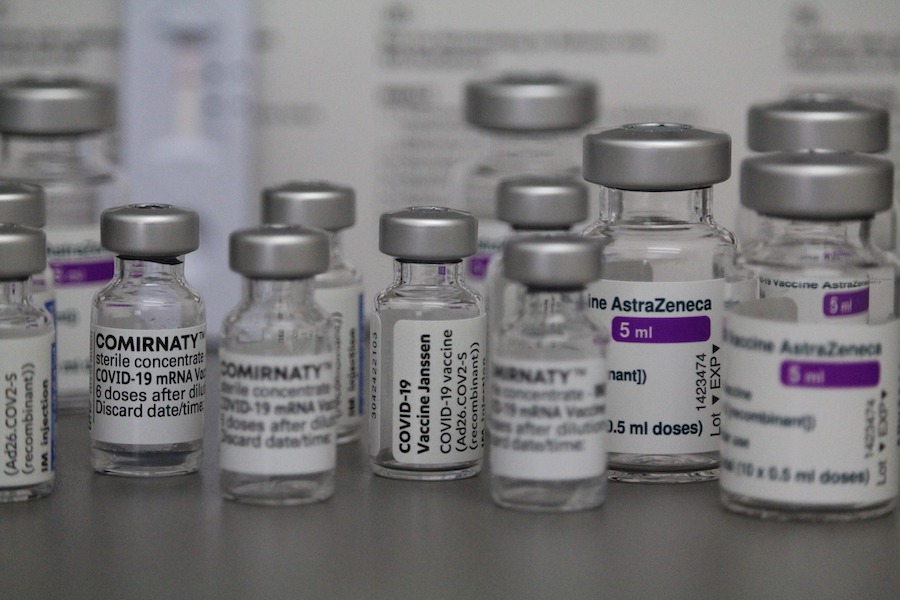
Les variants ne sont pas les seuls coupables
Comme l’écrit le Dr Peter Doshi, rédacteur en chef du BMJ, « les preuves de l’affaiblissement de l’immunité étaient déjà visibles dans les données à la date limite du 13 mars 2021. »
L’étude de Pfizer indique que « depuis son pic post-dose 2, la VE [efficacité du vaccin] observée, a diminué. De 7 jours à <2 mois après la dose 2, l’efficacité vaccinale était de 96,2 % (IC à 95 % [93,3-98,1]). De 2 mois à <4 mois, l’efficacité vaccinale était de 90,1 % (IC à 95 % [86,6-92,9]). Et de 4 mois à la date limite, l’efficacité vaccinale était de 83,7 % (IC à 95 % [74,7-89,9]). »
Peter Doshi estime que le point d’arrêt des données se situait approximativement un mois après le délai de quatre mois. En d’autres termes, selon les propres calculs de Pfizer, l’efficacité de son vaccin avait déjà baissé de 96,2 % à 83,7 % « jusqu’à six mois de suivi », soit environ cinq mois après la vaccination selon les calculs de Peter Doshi.
Il est à noter que Pfizer disposait déjà de ces informations supplémentaires en avril, mais qu’elles n’ont été « publiées que fin juillet ».
Bien que le variant Delta soit souvent tenu pour responsable de la baisse d’efficacité des vaccins, Peter Doshi affirme qu’« il est difficile d’imaginer comment le variant Delta pourrait jouer un rôle réel ici, car 77 % des participants à l’essai provenaient des États-Unis, où le variant Delta n’a été établi que plusieurs mois après l’arrêt des données. »
Les « propriétés intrinsèques du vaccin », ainsi que les nouveaux variants, et d’autres facteurs, pourraient tous avoir contribué à la perte d’efficacité. Ainsi, en l’absence de nouveaux essais cliniques démontrant l’efficacité des rappels sans augmenter le taux déjà alarmant d’effets indésirables graves, « il n’est pas certain que la série de deux doses réponde même à la norme d’approbation de la FDA à six ou neuf mois ».
Seulement 7 % des participants ont obtenu la levée de l’insu (la communication de l’identité d’un médicament camouflé) à six mois
L’essai contrôlé randomisé (ECR), qui est la référence absolue de la recherche sur l’efficacité, est « souvent réalisé en aveugle afin que les participants et les médecins, les infirmières ou les chercheurs ne sachent pas quel traitement chaque participant reçoit, ce qui limite encore le parti pris. » Cependant, l’étude de Pfizer présente un défaut majeur car : « seule la moitié des participants à l’essai (53 %) est arrivée au bout de quatre mois, et le suivi moyen est d’environ 4,4 mois. »
Peter Doshi explique : « Tout cela s’est produit parce qu’à partir de décembre dernier, Pfizer a accordé à tous les participants à l’essai la levée de l’insu, et aux bénéficiaires du placebo à se faire vacciner. Le 13 mars 2021 (date de clôture des données), 93 % des participants à l’essai (41 128 sur 44 060 ; figure 1) ont vu leur insu levée et sont entrés officiellement dans la phase de " suivi ouvert " ».
Pfizer a utilisé la terminologie « jusqu’à six mois » dans le titre de son étude au lieu de « à partir de six mois » parce que « seulement 7 % des participants à l’essai ont effectivement atteint six mois de suivi en aveugle. » Plus précisément, l’étude indique que « 8% des receveurs de BNT162b2 et 6% des receveurs de placebo ont eu un suivi ≥6 mois après la dose 2. »
Avec seulement 7% des participants à l’essai toujours suivis en aveugle au bout de six mois, ils ne constitueront probablement pas « un échantillon fiable ou valide pour produire d’autres résultats », a déclaré le Dr. Doshi.
Manque de transparence des données
La FDA a autorisé le vaccin Covid-19 de Pfizer « 13 mois après le début de l’essai pivot de deux ans qui est toujours en cours, sans qu’aucune donnée ne soit communiquée après le 13 mars 2021, avec une efficacité incertaine après six mois en raison de la levée de l’insu, des preuves d’une diminution de la protection indépendamment du variant Delta, et des rapports limités sur les données de sécurité », explique Peter Doshi.
Selon un article du BMJ, la FDA avait déclaré en août 2020 qu’elle était « engagée à utiliser un comité consultatif composé d’experts indépendants pour garantir que les délibérations sur l’autorisation ou la licence soient transparentes pour le public. » Toutefois, dans une récente déclaration au BMJ, la FDA a indiqué qu’« elle ne pensait pas qu’une réunion était nécessaire avant l’octroi prévu d’une autorisation complète. »
Une déclaration publique d’un groupe de plus de 30 cliniciens, scientifiques et défenseurs des patients a mis en évidence plusieurs questions ouvertes qui devaient être traitées avant l’approbation de tous les vaccins Covid-19. Malheureusement, l’étude préliminaire de Pfizer a abordé peu de ces questions et en a soulevé d’autres.
Le Dr. Peter Doshi stipule que la FDA devrait exhorter les entreprises à « compléter le suivi de deux ans, comme prévu à l’origine… exiger des études adéquates et contrôlées utilisant les résultats des patients dans la population désormais substantielle de personnes qui se sont remises de la Covid. Et les régulateurs devraient renforcer la confiance du public en veillant à ce que chacun puisse accéder aux données sous-jacentes. »
Rédacteur Fetty Adler
Soutenez notre média par un don ! Dès 1€ via Paypal ou carte bancaire.